MOHSEN AZAD
قـــــــــــــــــارچ شناســـــــــــــــــــــی پزشکــــــــــــــــــــی
جدیدترین مطالب
لینک های وب
آرشیو وبلاگ
درباره وب

ســــــــــــــــــــــــــــــــــــــــــــــــــــلامی
به گــــــــــــرمی نـــــــــــــفسهاتون..
محسن
فوق لیسانس مدیکال مایکولوژی
و ســـــــــــــاکن شهر تهـــــــــــــــــران
هـــــــــــــــــــــــــــــــــــــــــــــستم.
امیــــــــــــــــــــــــــــــــــــدوارم که
لحظـــــــــــــــــات خـــــــــوب و خوشی
را در وبـــــــلاگم سپـــــــــــــــری نمایید.
.
.
1388 دانشگاه علوم پزشکی قم - کارشناسی
1393 دانشگاه علوم پزشکی اصفهان - کارشناسی ارشد
........(_\.........
.../_)...) \........
../ (....(__)......
.(__)...oooO....
Oooo..............
.
گفتم غم تو دارم گفتا غمت سر آید گفتم که ماه من شو گفتا اگر برآید
گفتم ز مهرورزان رسم وفا بیاموز گفتا ز خوب رویان این کار کمتر آید
گفتم که بر خیالت راه نظر ببندم گفتا که شبرو است او، از راه دیگر آید
گفتم که بوی زلفت گمراه عالمم کرد گفتا اگر بدانی هم اوت رهبر آید
گفتم خوشا هوایی کز باد صبح خیزد گفتا خنک نسیمی کز کوی دلبر آید
گفتم که نوش لعلت ما را به آرزو کشت گفتا تو بندگی کن کو بنده پرور آید
گفتم دل رحیمت کی عزم صلح دارد گفتا مگوی با کس تا وقت آن درآید
گفتم زمان عشرت دیدی که چون سر آمد گفتا خموش حافظ کاین غصه هم سر آید
جستجوی وب
موضوعات وب
لینک های مفید
سيستم انعقادي
Plasma coagulation cascade
تعادلي
بين پروکواگولانها (فاکتوهاي انعقادي)، آنتيکواگولانها و خاصيت
فيبرينوليتيک در خون وجود دارد که موجب ميشود خون هميشه به صورت مايع
باقي بماند.اين عوامل در زمان مناسب قادرند ترومبوس ايجاد نمايند.
فعال شدن پروکواگولانها نهايتاً موجب:
1- تشکيل ترومبوس
2- ثابت نگهداشتن لختهي فيبرين ميشود.اين کار از 2 طريق صورت ميگيرد: راه خارجي (Extrinsic) و راه داخلي (Intrinsic). در راه خارجي ابتدا فاکتور VII به وسيلهي عامل نسجي در مجاورت کلسيم و فاکتورهاي ديگر فعال شده فاکتور X را تحريک کرده آبشار انعقادي را ايجاد مينمايد. در راه داخلي ابتدا فاکتور XI فعال شده سپس فاکتور IX فعال گرديده Coagulation cascade صورت ميگيرد (شکل1).
فاکتور
نسجي يک پروتئين پروکواگولان ميباشد که در حالت طبيعي تجلي داخل سلولي
ندارد و تماس آن با خون غيرمستقيم است تا اينکه صدمهاي به عروق آندوتليوم
وارد شود و به شکل فعال در ميآيد.
فاکتور X توسط فاکتور VIIa و فاکتور نسجي در مجاورت کلسيم فعال ميشود. اين فاکتور در کمپلکس پروترومبين اثر کرده ترومبين را ميسازد. فاکتور TF/VIIa در فعال کردن مقدار کم فاکتور IX موثر است.
فاکتور VIII با VWF در جريان خون به صورت ترکيب وجود دارد. در موقع صدمهي عروقي فاکتور ونويلبراند (VWF) پلاکتها را در محل صدمه به حالت چسبنده در ميآورد. VIII به راحتي توسط VWF به محل صدمه منتقل شده به گيرندهي پلاکتي يعني فسفوليپيد ميچسبد. فاکتور X فعال شده فاکتور VIII را در حضور فسفوليپيد سطح پلاکتي و کلسيم فعال مينمايد. فاکتور 8 و فاکتور 10 مجدداً فاکتور X را فعالتر مينمايند.
اين عمل در کمپلکس پروترومبين دخالت مينمايد.
ساير اعمال فاکتور X فعال، فعال کردن فاکتورهاي IX,V,II ميباشد (شکل 2).
عمل ضد انعقادي
رفع ادامهي انعقاد توسط 1-جريان خون 2-غير فعال نمودن فاکتورهاي انعقادي توسطAntithrombin، Protein C&S صورت ميگيرد.
جريان
خون فاکتورهاي فعال شده را از ناحيهي رگ صدمه ديده به کبد منتقل ميکند
تا در آنجا تخريب شوند علاوه بر آن سه فاکتور ضد انعقادي فوق فاکتورهاي
انعقادي تشکيل شده را منهدم کرده مانع از وسعت انعقاد ميشوند.
Antithrombin
که در کبد ساخته ميشود. ترومبين ملحق شده فعاليت آن را از بين ميبرد.
اين فاکتور ساير فاکتورهاي انعقادي ديگر را نيز از عمل باز ميدارد
(شکل3).
فعاليت فيبرينوليتيک
پلاسمين تنها پروتئين فيبرينوليتيک شناخته شده در خون است نوع فعال آن
يعني پلاسمينوژن توسط فعالکنندههاي متعدد پلاسمينوژن به وجود ميآيد.
اين عمل نهايتاً موجب ميشود که لختهي فيبرين ليز شده از پخش شدن و شدت
يافتن لختهي فيبرين جلوگيري شود تا رگ بازمانده صدمه به جريان خون وارد
نشود.
اثر فيبرينوليتيک اين ماده مانند Urokinase،Streptokinase در درمان حل کردن انسدادهاي شرياني کرونر و عروق محيطي و به ندرت وريدي به کار ميرود
در سالهای اخیر تحقیقات زیادی بر روی تمام جوانب سیستم انعقاد خون انجام
گرفته و با دستیابی فزاینده به فاکتورهای خالص انعقادی ، امکان مطالعه
مستقیم برهم کنشها و شرایط انجام آنها ، برای هر فاکتور خاصی فراهم شده
است. از آن طریق ، برهم کنشهای جدیدی مشخص شده است که از آن جمله میتوان
واکنشهای متقاطع که مسیرهای داخلی و خارجی انعقاد را بهم مربوط میکنند و
حلقههای مهم فیدبک منفی و مثبت که در مراحل مختلف روند آبشاری انعقاد
موثراند اشاره نمود. همچنین در چند سال گذشته ، برای بسیاری از فاکتورهای
انعقادی ، DNA مکمل ار راههای DNA نوترکیب مربوطه تهیه شده و ساختمان اولیه اسیدهای آمینه آنها تعیین شده است.
|
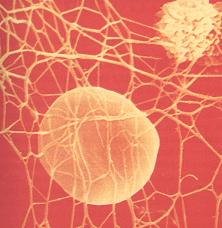
مکانیسم انعقاد
سیستم انعقاد خون با فعال شدن فاکتور XII یا VII و یا هر دو شروع میشود. اما هنوز معلوم نیست که فعال کننده خود اینها چیست. اینها هم موجب فعال شدن پروتئینی به نام ترومبینفیبرینوژن میشکند و ایجاد منومرهای فیبرینی میکند که متعاقبا به صورت یک لخته فیبرینی پلیمریک بسیار منظم درمیآیند.به علاوه ترومبین به عنوان یک محرک فیزیولوژیک بسیار قوی برای فعال شدن پلاکتها عمل میکند. پلاکتها در حضور یون کلسیم ، پروترومبین را به ترومبین تبدیل میکنند و همین باعث افزایش مقدار ترومبین و در نتیجه شدت واکنشها میگردد. نقطه پایان این واکنشها ، ایجاد پلیمر فیبرین است که هنوز قوام کمی دارد اما برهمکنشهای الکتروستاتیک ما بین مولکولهای منومر فیبرین مجاور ، باعث استحکام آن میشود.
پایدار شدن نهایی لخته خون با فعال شدن فاکتور XIII یا همان فاکتور پایدار کننده فیبرین صورت میگیرد که شامل ایجاد پیوند کووالانسی ما بین اسید آمینههای لیزین با گلوتامین بین زنجیرهای α و γ مجاور هم در مولکولهای فیبرین میباشد. نیز فاکتور XIII میتواند یک مهار کننده فیزیولوژیک فیبرینولیز را به لخته فیبرین با پیوند کووالانسی متصل میکند و در نتیجه لخته مربوطه در مقابل اثر لیزکنندگی پلاسمین حساسیت کمتری خواهد داشت. چنانچه در طی تشکیل لخته ، پلاکت باشد، لخته ایجاد شده کاملا جمع یا منقبض میشود و علت آن انقباض یک پروتئین پلاکتی است.
میگردند. تشکیل ترومبین یک حادثه بحرانی در روند انعقاد خون تلقی میشود. ترومبین مستقیما قطعات پپتیدی را از زنجیرههای α و β مولکول
|
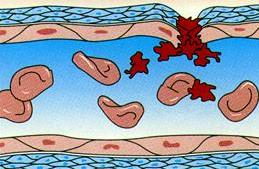
مهار کنندههای طبیعی انعقاد
- آنتی ترومبین III: با ترومبین به صورت یک به یک جمع شده و آن را از فعالیت باز میدارد.
- کو فاکتور IIهپارین: این نیز به عنوان مهار کننده ترومبین میباشد، کمبود ارثی این ، میتواند موجب ترامبوز شود.
- آلفا ماکروگلوبین: از جنس گلیکوپرتئین است و باز هم فعالیت ترومبین را باز میدارد.
- پروتئین C: وجود نیاز به ویتامین K دارد که بوسیله ترومبین فعال شده و موجب انعقاد میشود.
- پروتئین S: به عنوان کو فاکتور همراه پروتئین C عمل میکند و برای وجودش ، نیاز به ویتامین K است.
|
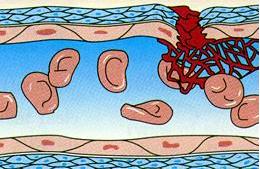
فیبرینولیز طبیعی
تشکیل لخته باعث قطع خونریزی از عروق صدمه دیده و مجروح میشود اما نهایتا باید برای برقراری مجدد جریان خون ، لخته ایجاد شده از سه راه برداشته شود. این عمل با حل شدن لخته بوسیله سیستم فیبرینولیتیک انجام میشود. آنزیمی به نام پلاسمین بطور متوالی برخی پیوندها را در مولکول فیبرین شکسته و باعث آزاد شدن محصولات پپتیدی و د ر نتیجه حل شدن لخته میشود. مکانیسمهای متعددی میتوانند در ایجاد پلاسمین فعال دخیل باشند که در همه آنها فاکتورهای خاص انعقاد موجب تبدیل این پروتئین از شکل غیر فعال به فعال میشود یعنی پلاسمینوژن به پلاسمین.اختلالات مادرزادی انعقاد خون
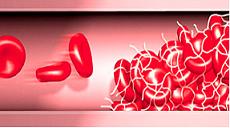
هموفیلی A
هموفیلی A ، شایعترین اختلال مادرزادی مربوط به فاکتورهای انعقادی است. که در اکثر کمبود فاکتور انعقادی VIII ایجاد میشود. ژن سازنده این پروتئین بر روی کروموزوم X فرد مبتلا قرار دارد و بنابراین ، در درجه اول ، مردان همیزیگوت را گرفتار میکند. با آنکه بطور معمول در ناقلین زن ، تمایل به خونریزی دیده نمیشود، اما مواردی هم وجود دارد که در زنان ناقل هم کمبود بالینی فاکتور VIII دیده میشود.این ناهنجاریهای ژنتیکی در افراد با فنوتیپ زنانه عبارتند از یک کروموزوم x ای که دارای ژن هموفیلی میباشد و فعال است. و در اثر غیر فعال شدن تصادفی کروموزوم X بطور افراطی (Extreme Lydnijtion) در زن هتروزیگوت
، X سالم غیرفعال شده است. تقریبا در 3/1 هموفیلیها نمیتوان سابقه خانوادگی هموفیلی را پیدا کرد و به نظر میرسد این به دلیل وجود چندین نسل ناقل خاموش یا وقوع یک جهش جدید است.
|
هموفیلی B
کمبود مادرزادی فاکتور IX یا هموفیلی B نیز ، اختلالی وابسته به کروموزوم X است و میزان شیوه آن حدودا 5/1 شیوع هموفیلی A است و از نظر تظاهرات بالینی ، قطعا نمیتوان بین هموفیلی A و B فرقی قائل شد. در هر دو ، خونریزیهای داخل مفصلی یا عضلانی ، خونریزی وسیع به دنبال عمل جراحی و عموما کبود شدگی آسان پوست میباشد. در هموفیلیها از علل عمده فوت ، وقوع خونریزی داخل جمجمهای است. هموفیلی B نیز اختلال وابسته کروموزوم X است.بیماری خون ویلبراند
این بیماری به صورت اتوزومی غالب منتقل میشود، اما در تعداد کمی از بیماران بنظر میرسد که به صورت اتوزومی مغلوب باشد. خونریزی در این بیماران ، مشخصا از پردههای مخاطی و نواحی جلدی است. در این بیماری با کمبود فاکتور VW مواجه هستیم که توسط سلولهای آندوتلیوم رگها و مگا کاریوسیتها ساخته میشوند و در پلاکتها ذخیره میگردند و در موقع لزوم ، از پلاکتها آزاد میگردد.درمان اختلالات مربوط به انعقاد خون
هم اکنون با بکار بردن روش RELP یکی از روشهای قوی از مهندسی ژنتیک به بودن یا نبودن این بیماریها میتوان در نسل بعد پی برد. همچنین |روش PCR ، توانسته است. با تولید پروتئینهای عامل انواع هموفیلی بعد جایگزینی این پروتئینها در گردش خون ، کمک شایانی به درمان این بیماریها بکند.موضوعات مرتبط: هماتولوژي
تاريخ : سه شنبه ۱۳۹۰/۰۹/۰۸ | 1:57 AM | نویسنده : محسن آزاد |
.: Weblog Themes By Pichak :.
پيوندهای روزانه
لینک های مفید
امکانات وب